作為壹種調節性T細胞固有的免疫檢查點,CTLA-4是壹把雙刃劍:它既能保護我們免受自身免疫性疾病之苦,卻又可能使癌癥逃避宿主的免疫監視。目前臨床上使用或正在研發階段的藥物雖然展現出良好的抗癌活性,但由於對免疫系統的調節作用減弱,導致相當壹部分癌癥患者出現了免疫治療相關不良事件(irAEs)。如何在兩種功能之間取得微妙的平衡,是癌癥免疫治療面臨的主要挑戰。
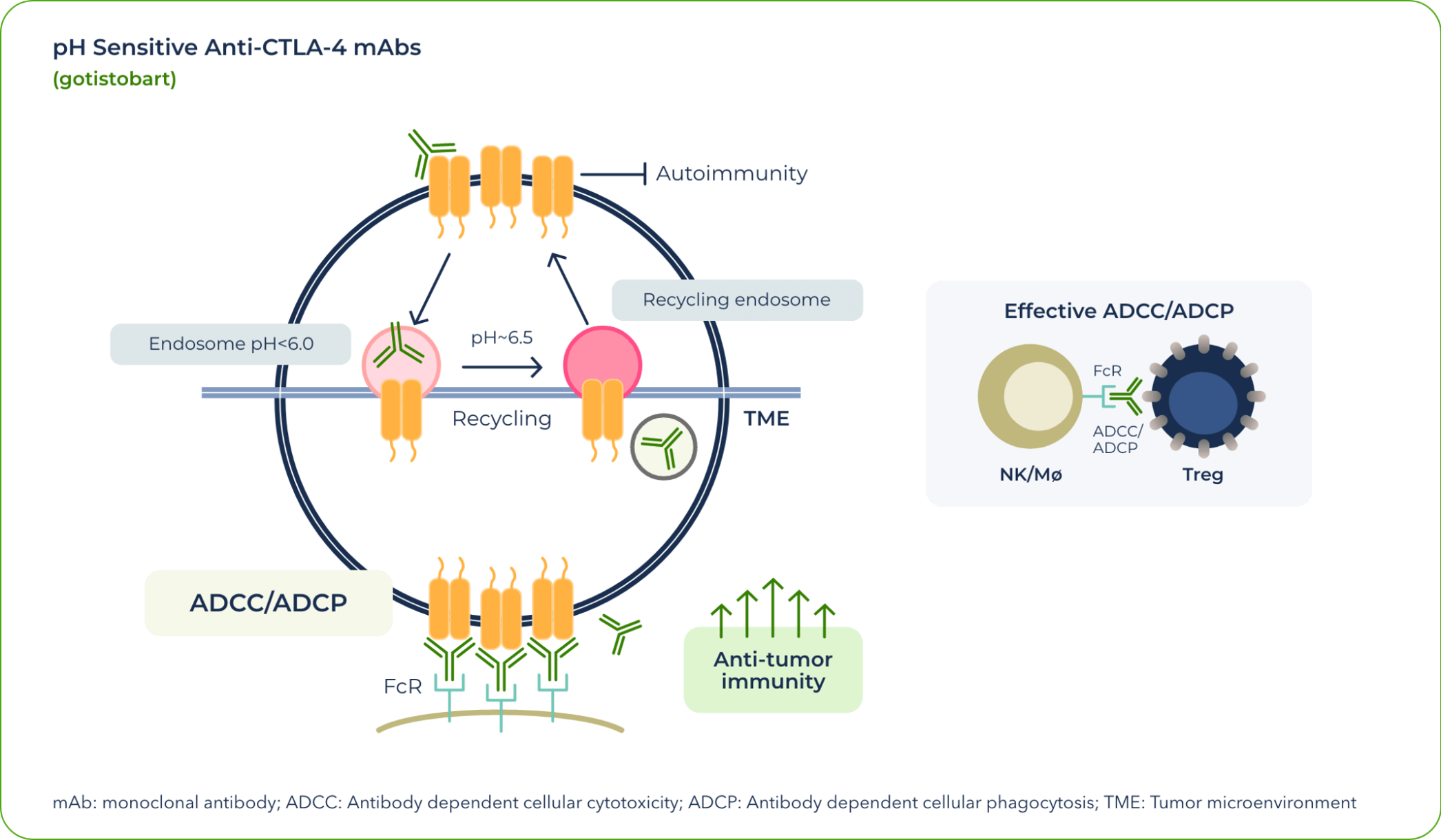
在目前獲批的利用CTLA-4通路的治療中,CTLA-4會在CTLA-4抗體將其拖入T细胞的溶酶體後降解。這意味著CTLA-4蛋白不再能被抗CTLA-4療法有效靶向調節性T細胞,降低了CTLA-4抗體的臨床活性。同時,目前獲批的抗體對CTLA-4免疫耐受檢查點的降解增加了其毒性。
我們團隊的研究發現,CTLA-4抗體對細胞外環境與細胞內環境的差異性pH敏感性對於保留CTLA-4蛋白至關重要,這壹重要見解是在開發gotistobart過程中獲得的。
當gotistobart在細胞表面與CTLA-4受體結合後,復合物會被內化。由於pH值的變化,兩者解離,使CTLA-4蛋白得以返回細胞表面,繼續在抗癌信號傳導中發揮作用。
實際上,gotistobart被設計為通過保留CTLA-4的循環來選擇性地耗竭腫瘤浸潤性調節性T細胞。1 在周圍組織中,保留CTLA-4的循環也保留了其控制自身反應性T細胞的能力,從而減少了免疫治療相關不良事件(irAEs)。
作為新壹代CTLA-4抗體,gotistobart由BioNTech和OncoC4共同進行臨床開發。
目前,gotistobart正在壹項進行中的1/2期臨床試驗PRESERVE-001(NCT04140526)中接受評估,該試驗在晚期實體瘤患者中研究gotistobart作為單藥或與帕博利珠單抗聯合使用的效果,同時還有壹項正在進行的註冊性3期臨床試驗PRESERVE-003(NCT05671510),該試驗評估gotistobart作為單藥治療在轉移性、免疫治療耐藥的非小細胞肺癌(NSCLC)患者中的效果。
Gotistobart在實體瘤患者以及那些先前接受過基於免疫治療方案且疾病進展的、無驅動突變的轉移性非小細胞肺癌患者中顯示出顯著的臨床活性。
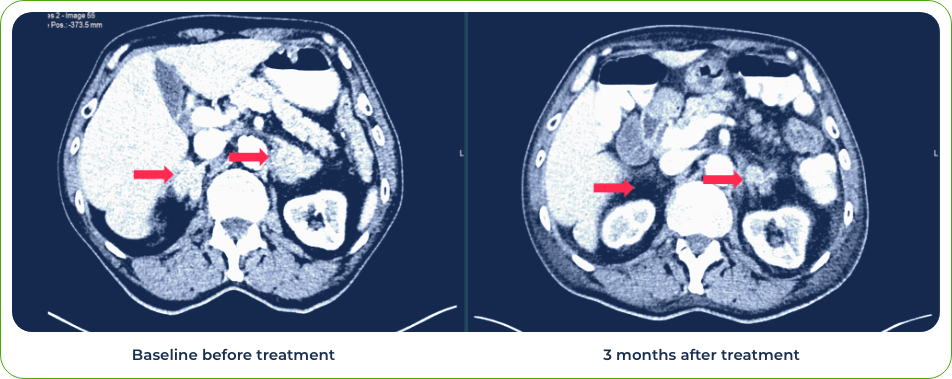
診斷:
IV期肺腺鱗癌
轉移部位:
腎上腺和大腦
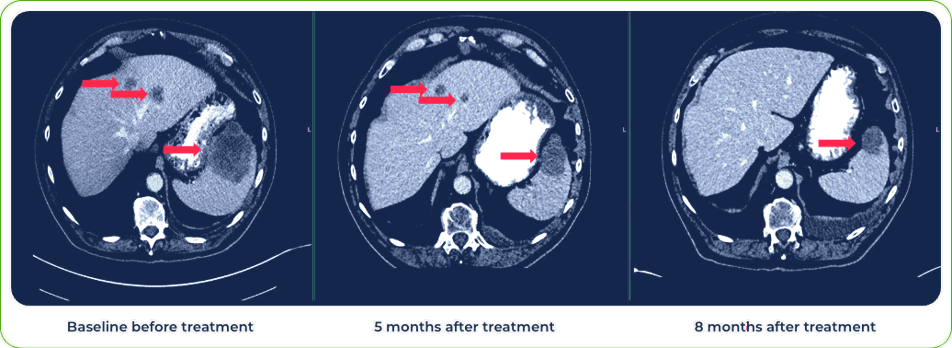
診斷:
IV期肺鱗狀細胞癌
轉移部位:
脾臟和肝臟
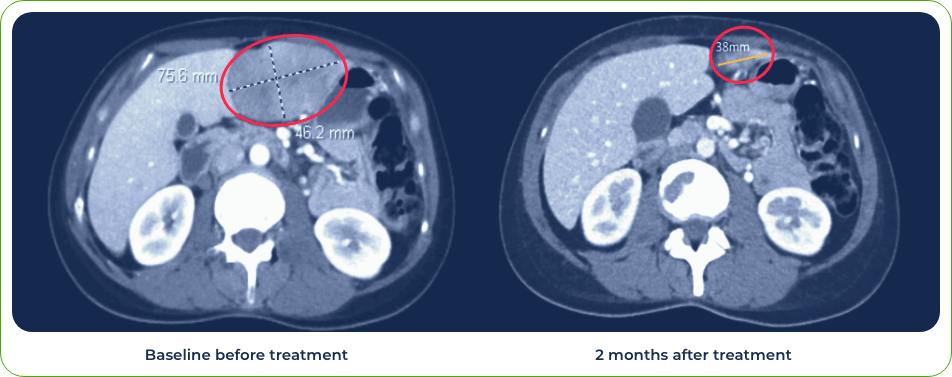
診斷:
IV期轉移性黑色素瘤
單劑量治療即誘導肝臟大型轉移病竈縮小

PD-1是另壹種作為T細胞“開關”的蛋白,有助於調節免疫系統。PD-1抑制劑通常與其他檢查點抑制劑聯合使用。
我們目前正在壹項2期臨床試驗中評估gotistobart與帕博利珠單抗聯合用於鉑耐藥卵巢癌的治療(NCT05446298)。它還在PRESERVE-006(NCT05682443)2期臨床試驗中與PLUVICTO®(鑥[177Lu]vipivotide tetraxetan)聯合用於評估治療,招募對象為接受過雄激素受體通路抑制劑和化療藥物紫杉醇類治療後疾病進展的轉移性去勢抵抗性前列腺癌患者。
1. Zhang Y, Du X, Liu M, Tang F, Zhang P, Ai C, Fields JK, Sundberg EJ, Latinovic OS, Devenport M, Zheng P, Liu Y. Hijacking antibody-induced CTLA-4 lysosomal degradation for safer and more effective cancer immunotherapy. Cell Res 2019 Aug;29(8):609-627. doi: 10.1038/s41422-019-0184-1


